Komórki macierzyste – obiecująca alternatywa dla przeszczepu wątroby w rzadkich chorobach
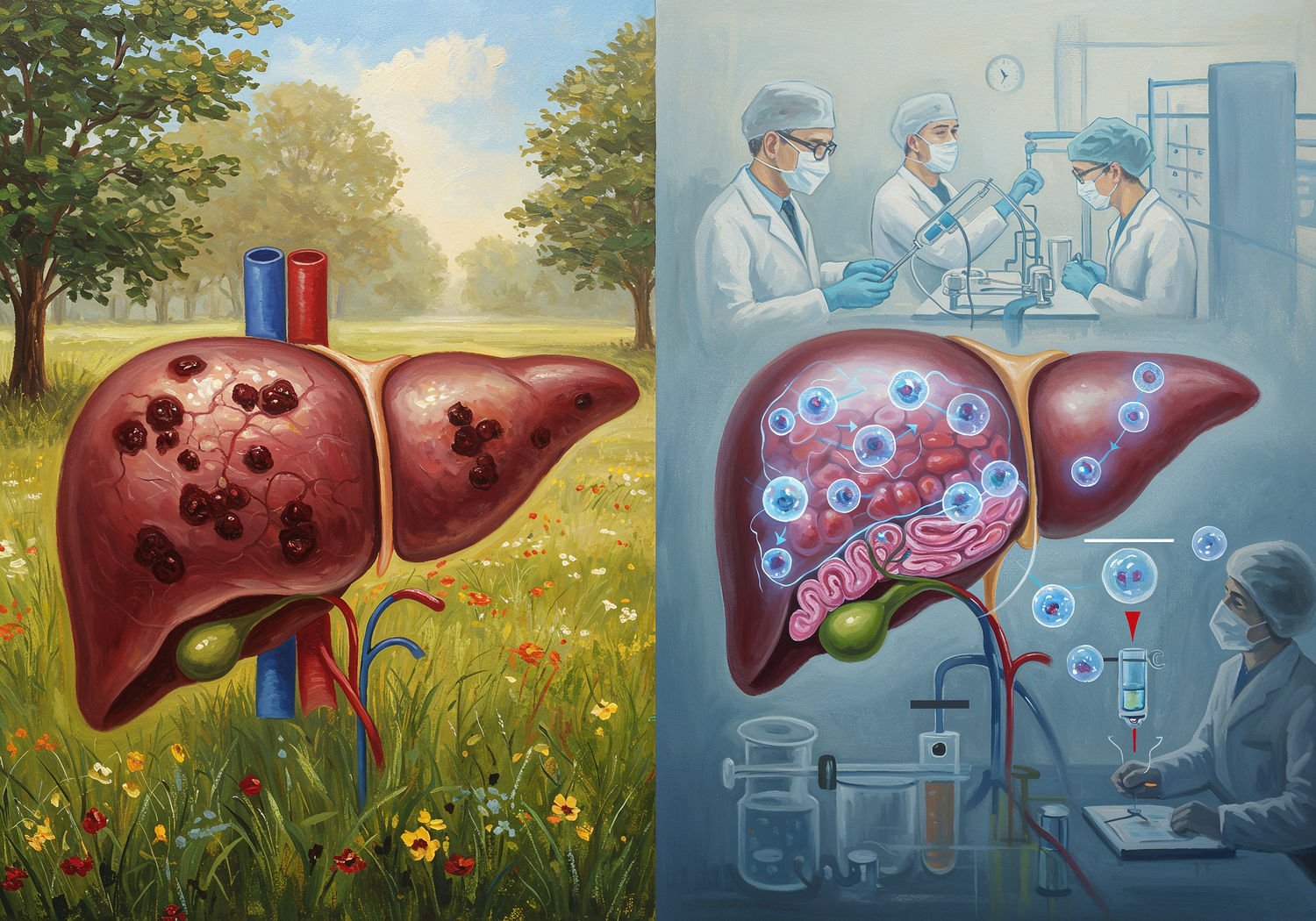
Wątroba to jeden z najbardziej regeneracyjnych organów w ludzkim ciele, ale w przypadku rzadkich chorób, takich jak zespół Criglera-Najjara czy choroba Wilsona, jej funkcje mogą być nieodwracalnie uszkodzone. Tradycyjnym rozwiązaniem jest całkowity przeszczep wątroby, jednak lista oczekujących jest długa, a dawcy rzadcy. Tutaj wkraczają komórki macierzyste, które otwierają drzwi do rewolucyjnych terapii. Ten artykuł przybliża, jak te wszechstronne komórki mogą wspierać regenerację wątroby, omawiając badania nad wyhodowanymi hepatocytami, technologię bio-sztucznej wątroby oraz wyzwania związane z ich wdrożeniem. W obliczu rosnącej liczby przypadków marskości i stłuszczenia wątroby, takie podejścia stają się nie tylko alternatywą, ale wręcz koniecznością dla milionów pacjentów na świecie.
Badania nad hepatocytami wyhodowanymi z komórek macierzystych – krok ku wsparciu uszkodzonego organu
Komórki macierzyste, zwłaszcza te indukowane pluripotencjalne (induced pluripotent stem cells, iPSCs), mają zdolność do przekształcania się w dowolny typ komórek, w tym hepatocyty – podstawowe komórki budujące miąższ wątroby. Badania nad nimi koncentrują się na stworzeniu laboratoryjnych odpowiedników naturalnych hepatocytów, które mogłyby przejąć funkcje uszkodzonego organu bez konieczności inwazyjnego przeszczepu.
W laboratoriach na całym świecie, w tym w instytucjach takich jak Uniwersytet w Tokio czy Mayo Clinic, naukowcy wyhodowali hepatocyty z iPSCs pacjentów z rzadkimi chorobami wątroby. Proces ten zaczyna się od pobrania komórek skóry lub krwi obwodowej, które są reprogramowane za pomocą czynników transkrypcyjnych, takich jak geny Oct4, Sox2, Klf4 i c-Myc. Następnie, w kontrolowanym środowisku z odpowiednimi czynnikami wzrostu, jak hepareina czy deksametazon, komórki różnicują się w hepatocyty zdolne do metabolizowania toksyn, produkcji białek osocza i detoksykacji organizmu.
Te wyhodowane hepatocyty wykazują aktywność enzymatyczną podobną do naturalnych, co potwierdzają testy in vitro. Na przykład, w modelach mysich z indukowaną marskością, infuzja takich komórek poprawiła poziomy albuminy i zmniejszyła stężenie bilirubiny. W kontekście rzadkich chorób, jak niedobór alfa-1-antytrypsyny, hepatocyty te mogłyby dostarczać brakujące białka bezpośrednio do krwiobiegu, omijając defektywną wątrobę. Badania kliniczne fazy I, prowadzone m.in. w Japonii, pokazują, że u pacjentów z ciężką niewydolnością wątroby, wstrzyknięte hepatocyty osiedlają się w narządzie i wspomagają jego funkcje przez tygodnie, co przedłuża życie w oczekiwaniu na przeszczep.
Jednak sukces zależy od efektywności integracji. Komórki macierzyste nie tylko zastępują uszkodzone hepatocyty, ale też wydzielają czynniki parakrynowe, takie jak hepatocyte growth factor (HGF), które stymulują podziały istniejących komórek wątroby. To podejście jest szczególnie obiecujące dla dzieci z rzadkimi zaburzeniami metabolicznymi, gdzie pełny przeszczep niesie ryzyko odrzutu i powikłań immunosupresyjnych.
Bio-sztuczna wątroba – most między kryzysem a ratunkiem dla oczekujących na dawcę
Technologia bio-sztuczej wątroby to hybrydowe urządzenie łączące elementy biologiczne z inżynierią, zaprojektowane jako tymczasowe wsparcie dla pacjentów w ostrej niewydolności wątroby. W przeciwieństwie do dializ dla nerek, ta innowacja wykorzystuje żywe komórki do pełnienia funkcji wątroby, działając jak most do transplantacji lub regeneracji.
Urządzenia takie jak Extracorporeal Liver Assist Device (ELAD) czy Bioartificial Liver Support System (BLSS) zawierają bioreaktor z hepatocytami wyhodowanymi z komórek macierzystych lub komórek świńskich. Krew pacjenta jest filtrowana przez membranę, gdzie komórki w bioreaktorze metabolizują amoniak, usuwa toksyny i syntetyzują białka. W badaniach klinicznych, np. tych prowadzonych przez firmę Vital Therapies, ELAD przedłużył życie pacjentów z ostrym uszkodzeniem wątroby o średnio 50%, umożliwiając regenerację naturalnej wątroby u 30% przypadków.
Dla rzadkich chorób, jak autoimmunologiczne zapalenie wątroby, bio-sztuczna wątroba może być dostosowana do specyficznych potrzeb, np. poprzez użycie pacjent-specyficznych iPSCs, co minimalizuje ryzyko reakcji immunologicznych. W fazie eksperymentalnej, systemy te integrują nanofibry lub hydrożele, które symulują mikrośrodowisko wątroby, poprawiając przeżywalność komórek do 80%. Pacjenci podłączeni do urządzenia przez 24-72 godziny odzyskują świadomość i stabilizują parametry życiowe, co jest kluczowe w sytuacji, gdy brak dawcy opóźnia przeszczep o miesiące.
Ta technologia nie leczy przyczyny, ale kupuje czas, stymulując naturalną regenerację. W kontekście globalnym, gdzie ponad 2 miliony ludzi rocznie umiera na choroby wątroby, bio-sztuczna wątroba mogłaby zmniejszyć śmiertelność na listach oczekujących o połowę, szczególnie w krajach o ograniczonym dostępie do transplantologii.
Infuzje komórek macierzystych – hamowanie włóknienia i pobudzanie regeneracji wątroby
Infuzja komórek macierzystych, głównie mezenchymalnych (mesenchymal stem cells, MSCs) z szpiku kostnego lub tkanki tłuszczowej, to nieinwazyjna metoda leczenia, która działa na dwóch frontach: hamuje postęp włóknienia i wspiera regenerację. Włóknienie wątroby, prowadzące do marskości, to nadmierne odkładanie kolagenu przez komórki hepatic stellate cells (HSCs), aktywowane przez cytokiny zapalne jak TGF-β.
MSCs, wstrzykiwane dożylnie lub bezpośrednio do tętnicy wrotnej, migrują do uszkodzonego narządu dzięki chemotaksji. Tam wydzielają czynniki przeciwzapalne, takie jak interleukina-10 i prostaglandyna E2, które dezaktywują HSCs i redukują produkcję macierzy pozakomórkowej. Badania na modelach zwierzęcych z marskością indukowaną tetrachlorkiem węgla wykazały, że pojedyncza infuzja MSCs zmniejsza włóknienie o 40-60% po 4 tygodniach, poprawiając przepływ krwi i funkcje metaboliczne.
W kontekście rzadkich chorób, jak hemochromatoza, MSCs stymulują hepatocyty do autoregeneracji poprzez sekrecję HGF i epidermal growth factor (EGF), co prowadzi do proliferacji komórek progenitorowych w kanalikach żółciowych. Kliniczne próby, np. w Chinach i USA, obejmujące ponad 200 pacjentów z marskością, pokazują poprawę wskaźnika MELD (Model for End-Stage Liver Disease) o 2-3 punkty po terapii, co opóźnia potrzebę przeszczepu. U pacjentów z stłuszczeniową chorobą wątroby (NAFLD), infuzje MSCs zmniejszają stan zapalny i akumulację tłuszczu, hamując ścieżkę NF-κB.
Proces regeneracji jest złożony: MSCs nie zawsze integrują się trwale, ale ich efekty parakrynowe trwają miesiące, dając wątrobie szansę na samonaprawę. To podejście jest bezpieczne, z niskim ryzykiem guzotwórczości, w przeciwieństwie do embrionalnych komórek macierzystych.
Wyzwania w terapii komórkowej – krążenie wrotne i dostarczanie do miąższu wątroby
Mimo obiecujących wyników, terapia komórkowa napotyka poważne przeszkody, szczególnie związane z anatomią wątroby. Krążenie wrotne, niosące 75% dopływu krwi do narządu, powoduje, że infuzowane komórki są szybko “przepłukiwane” przez zatokki wątrobowe, co ogranicza ich osiedlenie w miąższu do poniżej 5-10%.
Aby pokonać ten problem, naukowcy testują modyfikacje, jak powlekanie MSCs ligandami wiążącymi się z receptorami na śródbłonku sinusoidalnym, np. anty-CD44. W badaniach przedklinicznych, takie komórki wykazują 3-krotnie wyższą retencję. Inne podejście to embolizacja selektywna – wstrzykiwanie komórek przez cewnik do tętnicy wątrobowej, co zwiększa lokalne stężenie, ale niesie ryzyko niedokrwienia.
Dostarczanie do miąższu jest dodatkowo komplikowane przez barierę sinusoidalną i fibrozę, która blokuje migrację. W marskości, zwężone naczynia zmniejszają perfuzję, co prowadzi do nierównomiernego rozkładu komórek. Rozwiązaniem mogą być nośniki, jak mikropęcherzyki lub hydrożele, uwalniające MSCs stopniowo. Badania fazy II wskazują, że kombinacja infuzji z lekami przeciwfibrotycznymi, jak nintedanib, poprawia penetrację o 25%.
Bezpieczeństwo to kolejny aspekt: ryzyko tworzenia mikrozatorów w krążeniu wrotnym czy reakcji immunologicznych wymaga monitoringu. Mimo to, postępy w edycji genowej (CRISPR-Cas9) pozwalają na tworzenie “niewidzialnych” immunologicznie komórek, co może rozwiązać te wyzwania w ciągu dekady.
Globalne zapotrzebowanie na terapie oparte na komórkach macierzystych w erze rosnącej epidemii chorób wątroby
Światowa Organizacja Zdrowia szacuje, że do 2030 roku liczba przypadków marskości wątroby wzrośnie o 30%, napędzana otyłością, alkoholem i wirusowym zapaleniem wątroby. Stłuszczenie wątroby (MASLD) dotyka już 30% populacji dorosłych w krajach rozwiniętych, a rzadkie choroby, choć stanowią 5-10% przypadków, generują ogromne koszty – w USA przekraczają 1 miliard dolarów rocznie.
Terapie komórkowe wypełniają lukę, gdzie przeszczepy pokrywają tylko 10% potrzeb. W krajach rozwijających się, jak Indie czy Brazylia, gdzie dostęp do dawców jest minimalny, infuzje MSCs mogłyby uratować tysiące życia. Organizacje jak European Association for the Study of the Liver promują badania, podkreślając, że sukces w rzadkich chorobach, jak glikogenoza typu III, może być modelem dla powszechnych schorzeń.
Podsumowując, komórki macierzyste nie zastąpią całkowicie przeszczepów, ale jako alternatywa oferują nadzieję na personalizowane leczenie. Ich rozwój wymaga dalszych inwestycji, ale potencjał w hamowaniu epidemii chorób wątroby jest nieoceniony, dając pacjentom szansę na życie bez dializowej zależności od maszyny czy obcego organu.
Blog: MEDYCYNA I PROFILAKTYKA – Zdrowie i Uroda
Informacja: Artykuł (w szczególności treści i obrazy) powstał w całości lub w części przy udziale sztucznej inteligencji (AI). Niektóre informacje mogą być niepełne lub nieścisłe oraz zawierać błędy i/lub przekłamania. Publikowane treści mają charakter wyłącznie informacyjny i nie stanowią porady w szczególności porady prawnej, medycznej ani finansowej. Artykuły sponsorowane i gościnne są przygotowywane przez zewnętrznych autorów i partnerów. Redakcja nie ponosi odpowiedzialności za aktualność, poprawność ani skutki zastosowania się do przedstawionych informacji. W przypadku decyzji dotyczących zdrowia, prawa lub finansów należy skonsultować się z odpowiednim specjalistą.
Impressionist painting, plein air, vibrant colors, capturing the moment, flickering light, visible short brush strokes, broken color technique, soft focus A split-image illustration showing a damaged human liver on the left side with fibrosis and dark spots representing rare diseases, transitioning to a regenerating liver on the right side where glowing stem cells transform into healthy hepatocytes, integrate into the tissue, and release growth factors; in the foreground, a bio-artificial liver device connected to blood vessels filters toxins, while in the background, scientists in a lab infuse mesenchymal stem cells into a patient’s vein, symbolizing hope for patients awaiting transplants. ;Image without icons or texts. Style: Oil painting on canvas, impasto texture, thick layers of paint, high-key lighting, atmosphere of a hazy morning;