Komórki macierzyste w stomatologii – szansa na naturalne odrastanie zębów
Stomatologia od dawna zmaga się z wyzwaniami, takimi jak utrata zębów czy choroby przyzębia, które dotykają miliony ludzi na świecie. Ale co jeśli powiemy, że przyszłość leczenia zębów może opierać się nie na metalowych implantach czy syntetycznych wypełniaczach, lecz na naturalnej regeneracji? Komórki macierzyste, te niezwykłe “budulce” naszego organizmu, stają się kluczem do rewolucji w tej dziedzinie. W tym artykule przyjrzymy się, jak naukowcy wykorzystują komórki pochodzące z miazgi zęba do odbudowy tkanek jamy ustnej, na jakim etapie są badania nad hodowlą całych zębów i jak technologie takie jak druk 3D mogą zmienić wizyty u dentysty w coś więcej niż tylko borowanie.
Źródła komórek macierzystych w jamie ustnej – miazga zęba jako skarbnica potencjału
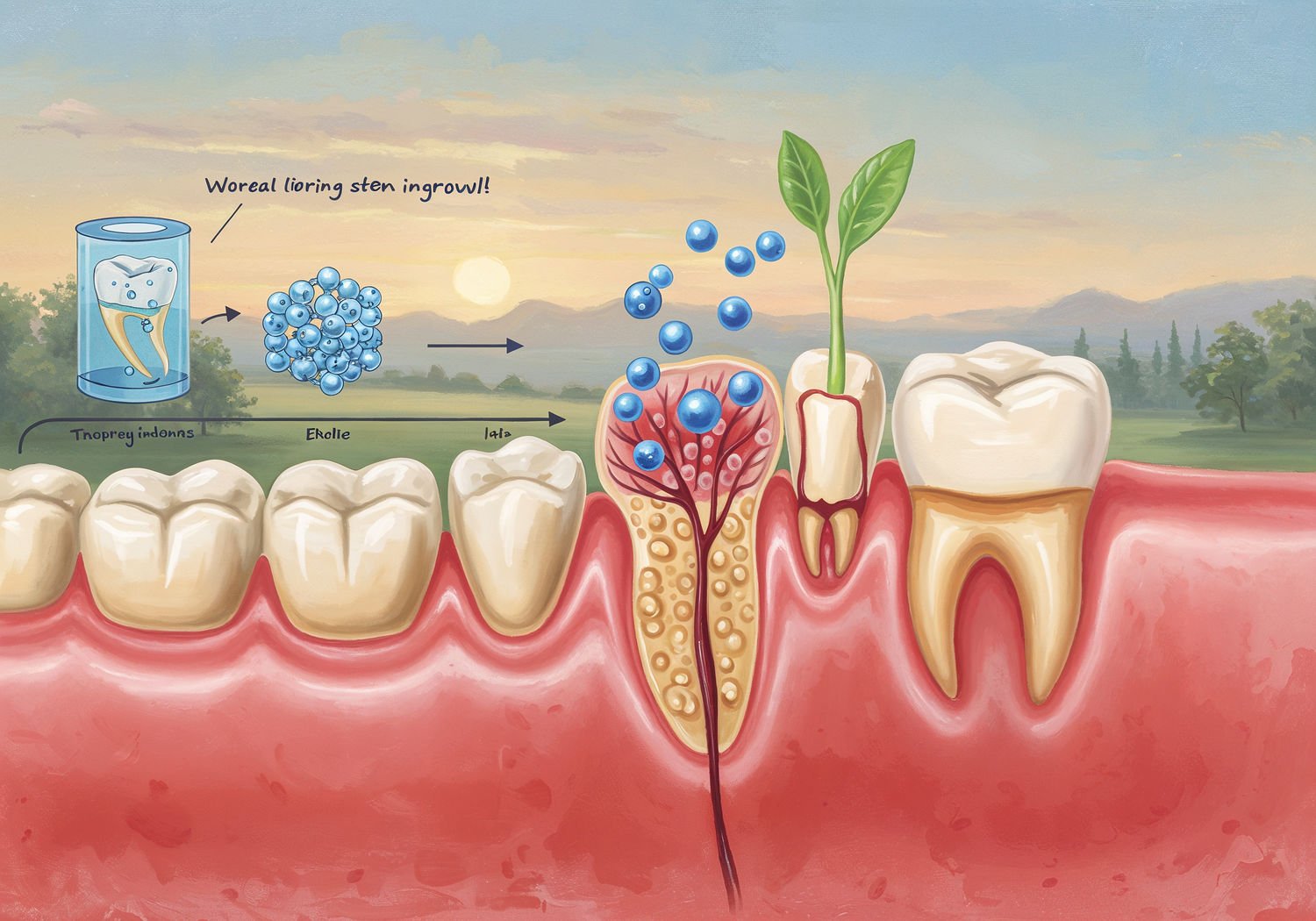
Komórki macierzyste to specjalne typy komórek, które mają zdolność do samoodnawiania się i różnicowania w różne rodzaje tkanek. W kontekście stomatologii szczególnie cenne są te izolowane z miazgi zęba, czyli tkanki wewnątrz zęba, składającej się z nerwów, naczyń krwionośnych i komórek produkujących dentinę. Miazga zęba, często usuwana podczas leczenia kanałowego, okazuje się bogatym źródłem komórek macierzystych miazgi zęba (dental pulp stem cells, DPSCs).
Te komórki są łatwe do pozyskania – wystarczy pobrać je z mlecznych zębów dzieci lub zębów mądrości u dorosłych, które i tak często są usuwane. Badania pokazują, że DPSCs mają unikalne właściwości: mogą przekształcać się w osteoblasty (komórki budujące kość), chondrocyty (tworzące chrząstkę) czy nawet neurony. To czyni je idealnymi do regeneracji struktur jamy ustnej, gdzie kości i tkanki łączne są narażone na codzienne obciążenia.
W praktyce klinicznej już dziś pobiera się te komórki i hoduje w laboratorium. Na przykład, w Japonii i USA trwają próby terapeutyczne, gdzie DPSCs wstrzykuje się w uszkodzone obszary dziąseł, by stymulować wzrost nowej tkanki. Proces ten opiera się na ich zdolności do wydzielania czynników wzrostu, takich jak vascular endothelial growth factor (VEGF), które wspomagają angiogenezę – tworzenie nowych naczyń krwionośnych. Dzięki temu rany goją się szybciej i naturalniej, bez ryzyka odrzutu, bo komórki pochodzą od samego pacjenta.
Jednak pozyskanie komórek to dopiero początek. Naukowcy muszą je “przekonać”, by różnicowały się w pożądany typ. Tu wkracza biologia molekularna: stosuje się czynniki takie jak bone morphogenetic proteins (BMP), które kierują rozwój ku kości lub dentinie. To nie science fiction – pierwsze sukcesy odnotowano w leczeniu paradontozy, gdzie DPSCs pomogły odbudować utracone przyzębie u pacjentów z zaawansowaną chorobą.
Regeneracja tkanek przyzębia i kości szczęki – od terapii wspomagającej do pełnej odbudowy
Choroby przyzębia, takie jak paradontoza, prowadzą do niszczenia tkanek podtrzymujących zęby, co kończy się ich ruchomością i utratą. Tradycyjne metody, jak przeszczepy kości czy sztuczne membrany, mają ograniczenia – często nie integrują się idealnie z organizmem. Tutaj komórki macierzyste oferują nadzieję na naturalną regenerację.
W badaniach na modelach zwierzęcych, np. u szczurów z sztucznymi ubytkami w kości szczęki, wstrzyknięcie DPSCs w połączeniu z rusztowaniami z hydrożelu (biokompatybilnych scaffoldów) pozwoliło na odbudowę kości w ciągu kilku tygodni. Komórki te nie tylko mnożą się, ale też wydzielają macierz pozakomórkową bogatą w kolagen, co wzmacnia strukturę. W klinice ludzkiej, w europejskich centrach jak Uniwersytet w Manchesterze, testuje się hybrydowe podejście: komórki macierzyste z miazgi miesza się z autologiczną kością pacjenta, by wypełniać ubytki po ekstrakcjach zębów.
Podobnie w regeneracji kości szczęki po urazach czy nowotworach. Komórki macierzyste z tkanki przyzębia (periodontal ligament stem cells, PDLSCs) są tu kluczowe – pochodzą z więzadeł otaczających zęby i mają naturalną tendencję do tworzenia cementu korzeniowego i kości wyrostka zębodołowego. Badania kliniczne fazy II, prowadzone m.in. w Korei Południowej, wykazały, że u 70% pacjentów z ciężką paradontozą nastąpiła znacząca poprawa – dziąsła przestały krwawić, a kieszonki periodontalne się zmniejszyły.
Wyzwaniem pozostaje integracja z istniejącymi tkankami. Naukowcy pracują nad optymalizacją dawek i kombinacjami z lekami immunosupresyjnymi, choć w przypadku autologicznych komórek ryzyko jest minimalne. Przyszłe terapie mogą łączyć DPSCs z terapią genową, by “włączać” geny odpowiedzialne za mineralizację, jak runt-related transcription factor 2 (RUNX2), kluczowy dla osteogenezy.
Hodowla całych zawiązków zębów – krok ku zamiennikom implantów
Marzeniem stomatologów jest hodowla kompletnych zębów, które rosłyby jak naturalne, zastępując drogie i inwazyjne implanty tytanowe. Badania nad tym trwają od lat 90., ale ostatnie lata przyniosły przełomy. Kluczowe są komórki macierzyste wyrostka zębodołowego (dental follicle stem cells, DFSCs), pozyskiwane z woreczków zębowych – struktur embrionalnych otaczających zawiązki zębów.
W laboratorium naukowcy, tacy jak japońscy badacze z Instytutu Medycyny Regeneracyjnej w Kioto, hodują te komórki w bioreaktorach, symulujących warunki jamy ustnej. Dodając sygnały molekularne, jak Wnt signaling pathway, kierują rozwój ku formowaniu zęba: od szkliwa po miazgę. W 2023 roku opublikowano wyniki eksperymentów na świniach, gdzie przeszczepione bio-zęby zintegrowały się z szczęką, tworząc korzeń i nerwobłoniarstwo.
Etap prac? Jesteśmy na styku badań przedklinicznych i wczesnych prób ludzkich. W Chinach i USA trwają studia fazy I, gdzie u pacjentów po ekstrakcji wszczepia się scaffold z DFSCs, by stymulować wzrost nowego zęba. Sukces? Wstępne dane wskazują na 40-50% przypadków, gdzie obserwowano kiełkowanie zawiązków. Wyzwania to czas – hodowla trwa miesiące – i etyka pozyskiwania komórek z embrionów, choć coraz częściej używa się indukowanych pluripotencjalnych komórek macierzystych (induced pluripotent stem cells, iPSCs) z skóry pacjenta.
Gdy to zadziała, implanty staną się reliktem. Naturalny ząb będzie rósł, dostosowując się do sił żucia, bez ryzyka periimplantitis – zapalenia wokół sztucznych korzeni.
Druk 3D z biotuszy – precyzyjne budowanie struktur jamy ustnej
Technologia druku 3D rewolucjonizuje stomatologię, a połączenie jej z komórkami macierzystymi otwiera erę bioprintingu. Biotusze to specjalne “atramenty” zawierające żywe komórki pacjenta, hydrożele i czynniki wzrostu, drukowane warstwa po warstwie w precyzyjne struktury.
W praktyce, dla regeneracji kości szczęki, drukuje się rusztowania z biotuszy na bazie alginianu sodu, nasączone DPSCs. Urządzenia jak te od firmy Organovo pozwalają na tworzenie porowatych szkieletów, które komórki kolonizują, tworząc nową kość. Badania w Wake Forest Institute for Regenerative Medicine pokazały, że takie bioprintowane implanty u psów zregenerowały 80% ubytku w szczęce po 6 miesiącach.
W leczeniu przyzębia bioprinting umożliwia drukowanie mini-organoidów – miniaturowych modeli tkanek – z PDLSCs i fibroblastami. Te struktury wszczepia się bezpośrednio w kieszonki, gdzie integrują się z dziąsłami. Zalety? Personalizacja: skan 3D jamy ustnej pozwala na idealne dopasowanie.
Jednak technologia jest wciąż rozwijana. Problemy to żywotność komórek podczas druku (muszą przetrwać ciśnienie) i biokompatybilność tuszy. Przyszłe wersje mogą obejmować druk całych zębów, z warstwami szkliwa i dentyny, co skróci czas terapii z lat do miesięcy.
Przyszłość stomatologii – od borowania do biologii molekularnej
Wyobraź sobie wizytę u dentysty, gdzie zamiast wiertła używa się skanera i iniekcji komórek. To nie odległa przyszłość – eksperci szacują, że w ciągu 10-15 lat regeneracyjna stomatologia stanie się standardem. Już dziś w Szwecji i Singapurze kliniki oferują terapie z DPSCs na paradontozę, a hodowla zębów może być dostępna w latach 2030.
Zmiana ta opiera się na biologii molekularnej: edycja genów za pomocą CRISPR-Cas9 pozwoli na “programowanie” komórek do szybszej regeneracji. Ryzyka? Koszty początkowe i potrzeba regulacji, ale korzyści – mniej bólu, naturalne efekty – przeważają.
Dziś borowanie to konieczność, ale jutro dentystyka będzie ożywiać, nie zastępować. Komórki macierzyste to most między tym, co znamy, a tym, co możliwe – naturalne odrastanie zębów może stać się rzeczywistością. Warto śledzić te badania, bo zmieniają nie tylko uśmiech, ale całe nasze zdrowie.
Blog: MEDYCYNA I PROFILAKTYKA – Zdrowie i Uroda
Informacja: Artykuł (w szczególności treści i obrazy) powstał w całości lub w części przy udziale sztucznej inteligencji (AI). Niektóre informacje mogą być niepełne lub nieścisłe oraz zawierać błędy i/lub przekłamania. Publikowane treści mają charakter wyłącznie informacyjny i nie stanowią porady w szczególności porady prawnej, medycznej ani finansowej. Artykuły sponsorowane i gościnne są przygotowywane przez zewnętrznych autorów i partnerów. Redakcja nie ponosi odpowiedzialności za aktualność, poprawność ani skutki zastosowania się do przedstawionych informacji. W przypadku decyzji dotyczących zdrowia, prawa lub finansów należy skonsultować się z odpowiednim specjalistą.
Impressionist painting, plein air, vibrant colors, capturing the moment, flickering light, visible short brush strokes, broken color technique, soft focus A cross-section view of a human jaw showing a damaged tooth socket being regenerated by stem cells: dental pulp stem cells extracted from a wisdom tooth are injected into the area, forming new bone, periodontal ligament, and a budding tooth structure emerging naturally, with subtle elements of a 3D bioprinter nearby depositing bio-ink scaffolds, and a timeline arrow indicating progression from extraction to full regrowth. ;Image without icons or texts. Style: Oil painting on canvas, impasto texture, thick layers of paint, high-key lighting, atmosphere of a hazy morning;